Kapcsolatba lépni:Errol Zhou (Úr.)
Tel: plusz 86-551-65523315
Mobil/WhatsApp: plusz 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
Email:sales@homesunshinepharma.com
Hozzáadás:1002, Huanmao Épület, No.105, Mengcheng Út, Hefei Város, 230061, Kína
Az AstraZeneca nemrégiben jelentette be, hogy az Európai Gyógyszerügynökség (EMA) emberi felhasználásra szánt gyógyszerek bizottsága (CHMP) pozitív értékelést adott ki, amely azt javasolja, hogy a célzott rákellenes gyógyszer, a Koselugo (szelumetinib) feltételesen jóváhagyásra kerüljön. Új típusú orális kináz-gátló tüneti, nem rezekálható plexiform neurofibroma (PN) kezelésére 1. típusú neurofibromatosisban (NF1) szenvedő gyermekkorú betegeknél. Most a CHMP véleményeit felülvizsgálatra benyújtják az Európai Bizottsághoz (EB), amely várhatóan a következő két hónapban hoz végleges felülvizsgálati döntést. Jóváhagyása esetén a Koselugo lesz az első gyógyszer, amely Európában kezeli az NF1-et.
Az NF1 az idegrendszer legyengítő genetikai betegsége, globálisan 3000 esetenként egy eset fordul elő. Az NF1 betegek 30-50% -ában a daganat az ideghüvelyen fordul elő (plexiform neurofibroma [PN1]), ami olyan klinikai problémákat okozhat, mint: diszfiguráció, légúti diszfunkció, látásromlás, hólyag- / bélműködési zavar.
2020 áprilisában az USA FDA jóváhagyta a Koselugot az NF1-hez kapcsolódó tüneti, működésképtelen plexiform neurofibromák (PN) kezelésére ≥2 éves NF1-es gyermekkorú gyermekekben. Érdemes megemlíteni, hogy a Koselugo az első olyan gyógyszer, amelyet az amerikai FDA jóváhagyott az NF1 kezelésére. Korábban a Koselugo ritka betegségek gyógyszermegjelölését (ODD) és áttörő gyógyszerjelölését (BTD) kapta az NF1 kezelésére. A Koselugo kinázinhibitor, ami azt jelenti, hogy kulcsfontosságú enzimeken keresztül képes megakadályozni a tumorsejtek növekedését.
A CHMP pozitív véleményei a II. Fázisú SPRINT Stratum 1 vizsgálat eredményein alapulnak. Ez egy próba, amelyet a National Cancer Institute (NCI) Cancer Treatment Evaluation Project (CTEP) támogat. A vonatkozó eredményeket a legfelsõbb nemzetközi orvosi folyóirat, a&idézte; New England Journal of Medicine GG; (NEJM), lásd: Selumetinib inoperábilis plexiformos gyermekeknél.
Az adatok azt mutatják, hogy a Koselugo (szájon át, naponta kétszer) monoterápia jelentős klinikai előnyökkel jár a betegek számára: folyamatosan csökkentheti a daganat méretét, enyhítheti a fájdalmat, javíthatja a napi funkciókat és az egészséggel kapcsolatos általános életminőséget. Ebben a vizsgálatban a Koselugo-kezelés objektív válaszaránya (ORR) 66% volt, és 50 betegből 33 megerősítette a részleges válaszokat. Az ORR a tumor térfogatának legalább 20% -kal történő csökkenése.
Az NF1 egy ritka betegség, amely gyengít, progresszív és gyakran torzító hatású. Ez a betegség általában az élet elején kezdődik, és specifikus gének mutációi vagy hibái okozzák. Az NF1-et általában kora gyermekkorban diagnosztizálják. Az NF1 körülbelül 3000 minden csecsemőben van jelen, amelyet a bőr színének (pigmentációja), az ideg- és csontkárosodás, valamint a jóindulatú és rosszindulatú daganatok kialakulásának kockázata jellemez az egész életen át. Az NF1-ben szenvedő betegek 30-50% -ának van egy vagy több plexiform neurofibromája (PN). A PN fő kezelése a műtéti reszekció. Sajnos ezen daganatok helye vagy mennyisége miatt sok beteg nem alkalmas műtétre. Ezenkívül az NP általában az optimális műtéti reszekció után kiújul, ezért a kielégítetlen orvosi szükségletek fontos területét jelenti.
A SPRINT Stratum 1 vizsgálatba 50 gyermek beteget vontak be (medián életkor 10,2 év, tartomány: 3,5-17,4), ezeknek a gyerekeknek NF1 és inoperábilis PN-je volt (definiálva hiányos reszekció, de nem jelentene komoly kockázatot a beteg PN-jére). A leggyakoribb neurofibromákkal kapcsolatos tünetek a diszfiguráció (44 eset), a motoros diszfunkció (33 eset) és a fájdalom (26 eset). A vizsgálat során a betegek naponta kétszer szedtek 25 mg / m2 (jóváhagyott ajánlott adag) Koselugo-t, amíg az állapot súlyosbodott vagy elfogadhatatlan mellékhatások jelentkeztek. A vizsgálat során rutinszerűen értékelték a beteg daganatmennyiségének változását és a daganattal kapcsolatos betegség tüneteit, és meghatározták az általános válaszarányt (ORR), amelyet teljes vagy részleges válaszként definiáltak MRI-vel 3-6 hónap alatt (PN tumor térfogata). csökkenés ≥ 20%) a betegek aránya.
Az NEJM-en közzétett adatok azt mutatják, hogy 2019. március 29-én az 50 beteg közül 35-en megerősítették a remissziót, vagyis a Koselugo orális monoterápia napi kétszeri teljes remissziós aránya (ORR) 70% (n=35) / 50 ), minden beteg részleges remisszióban (PR) szenvedett. A megerősített remisszióban szenvedő 35 beteg közül 28 (80%) tartós remissziót mutatott (remisszió időtartama ≥ 1 év).
Ezenkívül a vizsgálat azt is értékelte, hogy a Koselugo milyen hatással van a betegek egyéb klinikai eredményeire, ideértve a PN-vel kapcsolatos hibák, tünetek és funkcionális károsodások változását. Bár az egyes PN-vel kapcsolatos morbiditást (például hibák, fájdalom, erő és mozgásproblémák, légúti kompresszió, látásromlás, valamint hólyag- vagy bélműködési zavarok) értékelő betegek mintanagysága kicsi, a kezelés során a PN-vel kapcsolatos hibák, tünetek és funkciók kár is javulást mutatott.
Konkrétan: 1 éves kezelés után a betegek által jelentett daganat fájdalomintenzitási pontszáma átlagosan 2 ponttal csökkent, ami klinikailag jelentős javulásnak tekinthető. Ezenkívül a gyermekek és a szülők által jelentett napi funkció (38, illetve 50%) és az egészséggel összefüggő általános életminőség (48, illetve 58%), valamint az erő funkciói (56%), ill. mozgástartomány (38%) Az eredményben klinikailag jelentős javulás is megfigyelhető volt.
A 3 éves követés után a betegség progresszió nélküli túlélési aránya a Koselugo kezelési csoportban 84% volt, szemben a betegség természetes kórtörténetében szereplő kontrollcsoportban csak 15% -kal. A vizsgálat során 5 beteg abbahagyta a kezelést a Koselugóval kapcsolatos lehetséges toxikus hatások miatt, és 6 beteg' állapota romlott. A leggyakoribb toxikus reakciók az émelygés, hányás, hasmenés, a kreatin-foszfokináz szint tünetmentes emelkedése, pattanásszerű kiütések és paronychia.
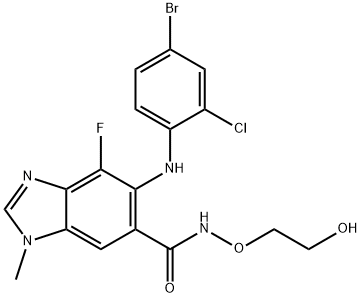
A Koselugo' selumetinib hatóanyag molekuláris szerkezete (képforrás: chemicalbook.com)
A Koselugo hatóanyaga a szelumetinib, amely egy orális, erős és szelektív MEK1 / 2 kináz inhibitor. Az NF1 gén a neurofibromint (neurofibromin) kódolja, amely negatívan szabályozza a RAS / MAPK útvonalat, és segít szabályozni a sejtek növekedését, differenciálódását és túlélését. Az NF1 gén mutációi a RAS / RAF / MEK / ERK jelátviteli út diszregulációjához vezethetnek, ami a sejtek kontrollálatlan növekedését, osztódását és szaporodását okozhatja, és tumor növekedéshez vezethet. A selumetinib potenciálisan gátolja a tumor növekedését azáltal, hogy gátolja a MEK enzimet ezen az úton. Jelenleg a selumetinibet egyetlen szerként kezelik, és más terápiákkal kombinálják a daganatok több típusának kezelésére a klinikai vizsgálatok során.
A selumetinibet az Array BioPharma fedezte fel, és az AstraZeneca 2003-ban engedélyezte a vegyület világszintű kizárólagos jogait. 2018 júliusában az AstraZeneca és a Merck onkológiai stratégiai együttműködésre tett szert a selumetinib és a PARP inhibitor Lynparza globális fejlesztése és forgalmazása érdekében. Jelenleg a két fél az I / II. Fázisú klinikai kutatást végzi a SPRINT segítségével, hogy feltárja a selumetinib potenciális előnyeit inoperábilis NF1-rel kapcsolatos plexiform neurofibromában (PN) szenvedő gyermekekben.